Старение, как сложный биологический процесс, который происходит на протяжении всей жизни, является основным фактором в развитии различных хронических заболеваний, особенно в значительной степени связанных с риском болезни Альцгеймера (БА). Однако его основные механизмы еще предстоит прояснить.
В нейрональном энергетическом метаболизме гуанозинтрифосфат (GTP), ключевая молекула, структурно подобная АТФ, не только участвует в клеточном энергоснабжении, но также играет жизненно важную роль в поддержании синаптической пластичности, транспорте везикул и регуляции аутофагии. Недавнее исследование, опубликованное в GeroScience командой Калифорнийского университета в Ирвине, под названием «Лечение возрастного снижения уровня ГТП восстанавливает эндоцитоз и аутофагию», показывает, что снижение уровня ГТП в нейронах во время старения ухудшает эндоцитоз и функции аутофагии.
Используя модель пожилой мыши, исследование показало, что комбинация добавок с никотинамидом (предшественником NAD +, формой витамина B3) и полифенолом зеленого чая EGCG (активатором Nrf2) восстановила уровни GTP в старых нейронах до молодых состояний в течение 16-24 часов. Это вмешательство не только значительно улучшило эндоцитоз и аутофагию, но также способствовало клиренсу β-амилоида и увеличило выживаемость нейронов на 22%, предлагая новый подход к вмешательству в нейродегенеративные заболевания, связанные со старением.

Исследовательская группа из Калифорнийского университета в Ирвине систематически анализировала изменения уровней ГТП в нейронах и их влияние на клеточную функцию в разных возрастных группах (молодые: 2-6 месяцев, средний возраст: 8-11 месяцев, старые: 17-28 месяцев) с использованием болезни Альцгеймера (AD). модельные мыши и мыши для контроля естественного старения. Используя флуоресцентные датчики для мониторинга уровня GTP в живых клетках в режиме реального времени, исследование показало, что:
Старение приводит к значительному снижению уровня GTP в нейронах (особенно в митохондриях), в то время как мыши с AD-моделью демонстрируют более серьезное снижение GTP уже в среднем возрасте, что позволяет предположить, что AD может ускорить дисфункцию энергетического метаболизма.
В качестве ключевого энергетического субстрата для аутофагии уровни GTP напрямую влияют на аутофагическую активность-ингибирование аутофагии приводит к накоплению GTP, тогда как активация аутофагии ускоряет потребление GTP.
С возрастом связанные с аутофагией ГТФазы (такие как Rab7 и Arl8b) аномально накапливаются в нейронах, что может быть связано с нарушением транспорта везикул, вызванным дефицитом ГТФ.
Комбинированное вмешательство с никотинамидом (предшественником NAD) и полифенолом зеленого чая EGCG (активатором Nrf2) может восстановить уровни GTP в старых нейронах до молодого уровня в течение 16-24 часов.
Это лечение значительно уменьшает количество и размер везикул Rab7/Arl8b-positive, демонстрируя его способность улучшать аутофагическую-лизосомальную функцию путем восстановления гомеостаза GTP.
Это исследование не только выявляет общие механизмы дисфункции энергетического метаболизма при старении и БА, но также предоставляет экспериментальные доказательства нейропротекторных стратегий, ориентированных на метаболизм GTP.
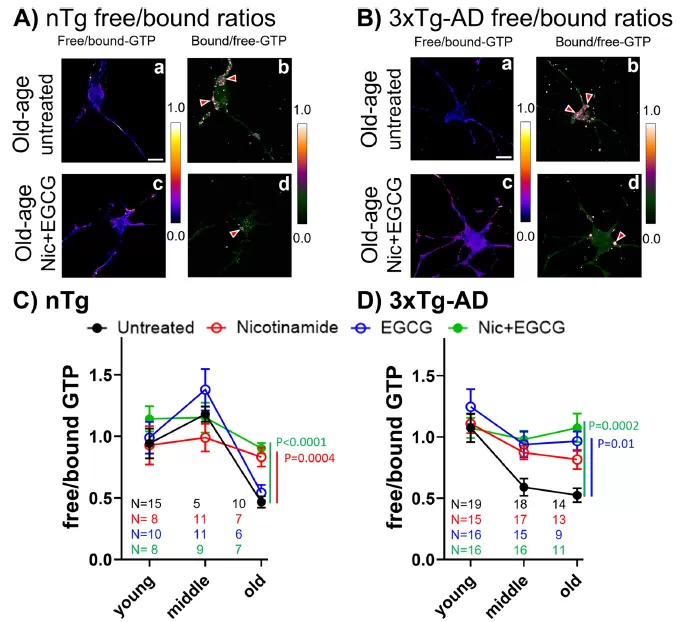
(Никотинамид + EGCG лечение восстанавливает нейрональные уровни GTP)
Кроме того, комбинированная терапия также способствовала клиренс внутриклеточного β-амилоидного белка, снижению уровня окисления белка и увеличению выживаемости нейронов на 22%. Эти результаты показывают, что восстановление уровней GTP облегчает клиренс Aβ и окислительно поврежденных белков.
Исследовательская группа отметила, что это исследование представляет собой первое систематическое выяснение критической регулирующей роли метаболизма GTP в старении и прогрессировании болезни Альцгеймера (AD). Однако, поскольку текущие исследования в основном основаны на экспериментах с клетками in vitro, их клинический перевод все еще требует дальнейшей проверки с помощью моделей на животных и клинических испытаний на людях.
Примечательно, что недавняя клиническаяИсследование, проведенное Калифорнийским университетом, показало, что перорально вводимый никотинамид склонен к биоинактивации в кровотоке, ограничивая его терапевтическую эффективность. Этот вывод предполагает, что будущие исследования должны оптимизировать методы доставки лекарств или разработать более стабильные системы доставки лекарств для повышения эффективности лечения.
Несмотря на эти проблемы, данное исследование имеет значительную теоретическую ценность. Это не только раскрывает центральную роль гомеостаза GTP при нейродегенеративных заболеваниях, но и закладывает научную основу для разработки новых стратегий вмешательства. Эти открытия обеспечивают потенциальные терапевтические цели для задержки, остановки или даже обращения вспять патологических процессов старения и БА.
Ссылки:
https://doi.org/10.1007/s11357-025-01786-4